| Formic acid | |
|---|---|
 |
|
| General | |
| Systematic name | Methanoic acid |
| Other names | Hydrogen carboxylic acid Formylic acid Aminic acid |
| Molecular formula | CH2O2 HCOOH |
| SMILES | O=CO |
| Molar mass | 46.,0254 g/mol |
| Appearance | Colorless, fuming liquid |
| CAS number | |
| Properties | |
| Density and phase | 1.22 g/mL, liquid |
| Solubility in water | Miscible |
| Other solvents | Ethanol, acetone, ether |
| Melting point | 8.4°C (47.1°F) |
| Boiling point | 100.8°C (213.3°F) |
| Acidity (pKa) | 3.75 |
| Viscosity | 1.,57 cP at 26°C |
| Structure | |
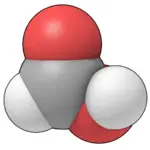
| Molecular shape | Planar |
| Dipole moment | 1.41 D(gas) |
| Hazards | |
| MSDS | ScienceLab.com |
| Main hazards | Corrosive; irritant; sensitizer.,68693″> 2
3
0
|
| Flash point | 69°C (156°F) |
| R-phrases | R10, R35 |
| S-phrases | S1/2, S23, S26, S45 |
| RTECS number | LQ4900000 |
| Supplementary data page | |
| Structure & properties | n, εr, etc.,haviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related carboxylic acids | Acetic acid Propionic acid |
| Related compounds | Formaldehyde Methanol |
| Except where noted otherwise, data are given for materials in their standard state (at 25°C, 100 kPa) |
|
Formic acid (systematic name methanoic acid) is the simplest carboxylic acid., Formula sa este HCOOH sau CH2O2. În natură, se găsește în înțepăturile și mușcăturile multor insecte din ordinul Hymenoptera, în special furnicile. În prezent, este utilizat ca conservant în hrana animalelor, ca intermediar în procesele chimice sintetice și ca ingredient activ în unele substanțe de îndepărtare a calcarului de uz casnic. Este, de asemenea, un produs semnificativ de ardere eliberat de vehiculele care rulează pe metanol amestecat cu benzină. O sare sau un ester al acidului formic se numește formiat sau metanoat. Ionul format are formula HCOO -.acest acid trebuie manipulat cu grijă., Contactul cu acidul formic lichid sau vaporii săi concentrați poate irita și deteriora pielea, ochii și tractul respirator.încă din secolul al XV-lea, unii alchimiști și naturaliști erau conștienți de faptul că dealurile furnicilor au dat vapori acide. În 1671, naturalistul englez John Ray a devenit prima persoană care a descris izolarea acidului formic prin distilarea unui număr mare de furnici. Aceste insecte secretă substanța în scopuri de atac și apărare. Astfel, numele „acid formic” a fost inventat din cuvântul Latin pentru furnică, formica.,acidul Formic a fost sintetizat pentru prima dată din acid cianhidric de către chimistul francez Joseph Gay-Lussac. În 1855, un alt chimist francez, Marcellin Berthelot, a dezvoltat o sinteză din monoxid de carbon, o metodă similară cu cea folosită astăzi.în industria chimică, acidul formic a fost mult timp considerat un compus de interes minor. Cu toate acestea, la sfârșitul anilor 1960, cantități semnificative din acesta au devenit disponibile ca produs secundar al producției de acid acetic. Acum este folosit din ce în ce mai mult ca conservant și antibacterian în hrana animalelor.,
proprietăți
acidul Formic este miscibil cu apa și majoritatea solvenților organici polari și oarecum solubil în hidrocarburi. Cele mai simple săruri de formiat sunt solubile în apă.când se dizolvă în hidrocarburi și când se află în faza de vapori, acidul formic constă mai degrabă din dimeri legați de hidrogen (perechi de molecule) decât din molecule individuale. În faza gazoasă, această legătură de hidrogen are ca rezultat abateri severe de la Legea ideală a gazului. În stările lichide și solide, acest acid constă dintr-o rețea de molecule legate de hidrogen., Când este încălzit, acidul formic se descompune în monoxid de carbon și apă.acidul Formic are majoritatea proprietăților chimice ale altor acizi carboxilici, dar prezintă și câteva proprietăți unice. De exemplu, în condiții normale, nu va forma nici o clorură de acil, nici o anhidridă acidă. Până de curând, toate încercările de a forma oricare dintre acești derivați au dus la monoxid de carbon. S-a demonstrat acum că anhidrida poate fi produsă prin reacția fluorurii de formil cu formiat de sodiu la -78°C., Clorura poate fi produsă prin trecerea HCl într-o soluție de 1-formimidazol în monoclormetan la -60°C. În plus, acidul formic împărtășește unele dintre proprietățile reducătoare ale aldehidelor.acidul Formic este unic printre acizii carboxilici în capacitatea sa de a participa la reacțiile de adiție cu alchene, producând esteri formiați. În prezența anumitor acizi, inclusiv acidul sulfuric și acidul fluorhidric, are loc totuși o altă reacție (o variantă a reacției Koch), în care acidul formic se adaugă la alchenă pentru a produce un acid carboxilic mai mare.,o cantitate semnificativă de acid formic este obținută ca produs secundar în fabricarea altor substanțe chimice, în special a acidului acetic. Deoarece această rută de producție este insuficientă pentru a satisface cererea actuală, un anumit acid formic trebuie produs de dragul său.când metanolul și monoxidul de carbon sunt combinate în prezența unei baze puternice, produsul este formiat de metil, un ester al acidului formic. Ecuația chimică poate fi scris ca:
CH3OH + CO → HCOOCH3
În industrie, această reacție se realizează în fază lichidă la presiune ridicată., Condițiile tipice de reacție sunt presiunea de 80°C și 40 atmosfere (atm). Cea mai utilizată bază este metoxidul de sodiu. Hidroliza de metil formiat produce acid formic:
HCOOCH3 + H2O → HCOOH + CH3OH
hidroliza Directă de metil formiat necesită un mare exces de apă pentru a continua eficient, și unii producători folosesc un indirecte traseu.în laborator, acidul formic poate fi obținut prin încălzirea acidului oxalic în glicerol anhidru, extragând produsul prin distilare cu abur., Un alt preparat (care trebuie efectuat sub o capotă de fum) este hidroliza acidă a izonitrilului de etil folosind soluție de acid clorhidric.
C2h5nc + 2H2O → C2H5NH2 + HCOOH
utilizări
utilizarea principală a acidului formic este ca conservant și agent antibacterian în hrana animalelor. Atunci când pulverizat pe fân proaspăt sau alte siloz, l arestări anumite procesele de descompunere și cauzele hrana să își păstreze valoarea nutritivă mai mult, și de aceea este utilizat pe scară largă pentru a păstra hrana de iarnă pentru vite. În industria păsărilor de curte, uneori se adaugă la hrană pentru a ucide bacteriile Salmonella.,
utilizări suplimentare:
- Este folosit pentru a procesa latex organic (sap) în cauciuc brut.
- apicultorii folosesc acidul formic ca miticid împotriva acarianului Varroa.
- este de o importanță minoră în industria textilă și pentru tăbăcirea pielii.unii esteri formati sunt arome artificiale sau parfumuri.
- este ingredientul activ în unele mărci de îndepărtare a calcarului de uz casnic.
- este utilizat în laboratoare ca modificator de solvenți pentru separările HPLC de proteine și peptide, în special atunci când proba este pregătită pentru analiza spectrometriei de masă.,
- în chimia organică sintetică, acidul formic este adesea folosit ca sursă a ionului de hidrură (prin reacția Eschweiler-Clarke sau reacția Leakart-Wallach) și ca sursă de hidrogen în ceea ce se numește „hidrogenare de transfer.”
- în laborator, acidul formic este utilizat ca sursă de monoxid de carbon, care este eliberat prin adăugarea de acid sulfuric. Este, de asemenea, o sursă pentru o grupare formil într-o reacție cunoscută sub numele de „formilare.,”
siguranță
principalul pericol cauzat de acidul formic este contactul cu pielea sau ochii cu acidul formic lichid sau cu vaporii concentrați. Oricare dintre aceste căi de expunere poate provoca arsuri chimice severe, iar expunerea ochilor poate duce la afectarea permanentă a ochilor. Vaporii inhalați pot provoca în mod similar iritații sau arsuri în tractul respirator. Deoarece monoxidul de carbon poate fi prezent și în vaporii de acid formic, trebuie avut grijă oriunde sunt prezente cantități mari de vapori de acid formic. U. S., Nivelul de expunere admisibil OSHA (PEL) de vapori de acid formic în mediul de lucru este de cinci părți la un milion de părți de aer (ppm).acidul Formic este ușor metabolizat și eliminat de organism. Cu toate acestea, unele efecte cronice au fost documentate. Unele experimente pe animale au demonstrat că este un mutagen, iar expunerea cronică poate provoca leziuni hepatice sau renale. O altă posibilitate cu expunere cronică este dezvoltarea unei alergii cutanate care se manifestă la re-expunerea la substanța chimică.pericolele soluțiilor de acid formic depind de concentrație.,ety symbol
| Concentration by weight |
Classification | R-Phrases |
|---|---|---|
| two to ten percent | Irritant (Xi) | R36/38 |
| 10–90 percent | Corrosive (C) | R34 |
| >90 percent | Corrosive (C) | R35 |
See also
- Acetic acid
- Acid
- Carboxylic acid
Notes
- Julius B., Cohen, Chimie Organică Practică (MacMillan, 1930).
- izonitrilul este obținut prin reacția etil aminei cu cloroform. Capota de fum este necesară din cauza mirosului excesiv de neplăcut al izonitrilului.
- L. F. Fieser și J. E. Jones, „N-methylformanilide” Sinteze Organice Coll. Vol. 3 (1955): 590; 20(1940): 66. Retrieved December 31, 2007.
toate link-urile preluate aprilie 19, 2017.,
- NIOSH Pocket Guide to Chemical Hazards: Formic Acid
credite
New World Encyclopedia scriitori și editori rescris și completat articolul Wikipedia în conformitate cu New World Encyclopedia standards. Acest articol respectă termenii licenței Creative Commons CC-by-sa 3.0 (CC-by-sa), care poate fi utilizată și difuzată cu atribuire corespunzătoare. Creditul se datorează în conformitate cu termenii acestei licențe care se poate referi atât la contribuitorii New World Encyclopedia, cât și la colaboratorii voluntari altruiști ai Fundației Wikimedia., Pentru a cita acest articol click aici pentru o listă de formate citând acceptabile.Istoria de mai devreme contribuții de wikipedians este accesibil cercetătorilor aici:
- acid Formic istorie
istoria acestui articol, deoarece acesta a fost importat la Noi Enciclopedia Lumii:
- Istoria „acid Formic”
Notă: se pot aplica Unele restricții la utilizarea de imagini individuale care sunt licențiate separat.
Leave a Reply