US Pharm. 2019; 44 (1): HS2-HS6.
ABSTRACT: L’ipertermia maligna è una sindrome clinica rara e pericolosa per la vita dell’ipermetabolismo che coinvolge il muscolo scheletrico. Negli individui sensibili, questa reazione è innescata principalmente dall’esposizione ad agenti anestetici inalatori volatili e succinilcolina (un rilassante muscolare)., Nei pazienti che sono suscettibili di ipertermia maligna, il recettore ryanodine nel muscolo scheletrico è anormale e provoca un accumulo di calcio nel muscolo scheletrico, con conseguente reazione metabolica massiccia dopo l’esposizione agli agenti scatenanti. L’ipertermia maligna deve essere trattata rapidamente per evitare un esito fatale. Nonostante la rarità dell’ipertermia maligna, le strutture sanitarie che utilizzano agenti scatenanti noti devono essere pienamente preparate per trattarla.
L’ipertermia maligna (MH) è un disturbo farmacogenico del muscolo scheletrico., Si manifesta come una crisi ipermetabolica pericolosa per la vita associata ad un aumento rapido e incontrollato del calcio mioplasmatico nei muscoli scheletrici. Questa crisi ipermetabolica è più spesso innescata in persone sensibili dalla somministrazione di anestetici volatili e dall’agente bloccante neuromuscolare succinilcolina.1,2
La suscettibilità MH è un tratto autosomico-dominante ereditato.2 Gli individui che sono suscettibili di MH hanno recettori ryanodine muscolo scheletrico anormale; questa anomalia interferisce con la regolazione del calcio nel muscolo., Quando un ricevitore anormale di ryanodine che controlla il rilascio del calcio è presente, un accumulo di calcio può accadere, piombo ad una reazione metabolica sostanziale sopra esposizione ad un agente di innesco.3-5
Indicazioni
In un paziente vivendo MH, la reazione provoca un aumento della produzione di anidride carbonica, metabolica e respiratoria, acidosi, l’accelerato consumo di ossigeno, produzione di calore, sistema nervoso simpatico attivazione, iperkaliemia, e coagulazione intravascolare disseminata (DIC), tutti risultanti in fallimento multisistemico., I primi segni clinici di MH sono ipercapnia (elevati livelli di anidride carbonica nel sangue), tachipnea, tachicardia e rigidità muscolare. I segni successivi possono includere ipertermia, alterazioni dell’ECG correlate all’iperkaliemia e mioglobinuria.6
Gli individui MH-suscettibili non possono sviluppare coerente la sindrome acuta una volta esposti agli anestetici. Una crisi MH può verificarsi alla prima esposizione a un agente scatenante; tuttavia, il paziente medio suscettibile all’MH ha avuto esposizioni precedenti prima che si verifichi una reazione documentata.,7 Una storia di anestesia senza eventi con agenti MH-triggering non dovrebbe escludere la suscettibilità a MH; episodi MH derivanti dall’uso di agenti presumibilmente sicuri sono stati segnalati anche.
Test diagnostici
Test per la suscettibilità MH è più utile nel prendere decisioni di trattamento per i pazienti chirurgici che possono essere suscettibili di MH. Il test diagnostico non è raccomandato come strumento di screening per la popolazione generale. I test diagnostici includono il test della contrattura caffeina-alotano e il test genetico (sequenziamento del gene del recettore ryanodine)., Il test della contrattura muscolare, che è considerato il gold standard, richiede una biopsia muscolo-scheletrica dalla coscia del paziente.8
Epidemiologia
Gli studi dimostrano che MH complica circa uno su 100.000 interventi chirurgici negli adulti e uno su circa 30.000 interventi chirurgici nei bambini.2 La vera incidenza della suscettibilità alla MH non è stata stabilita con precisione negli Stati Uniti a causa della mancanza di segnalazioni universali e del fatto che molte persone sensibili alla MH non sono state esposte a un agente scatenante. MH si verifica a livello globale in tutti i gruppi etnici., Le reazioni sono riportate più frequentemente negli uomini che nelle donne, e i pazienti di età inferiore ai 19 anni rappresentano circa il 50% degli eventi segnalati.6,7
Agenti scatenanti
Nel corso degli anni, un certo numero di farmaci sono stati implicati come trigger MH. Secondo l’Associazione Ipertermia maligna degli Stati Uniti (MHAUS), i seguenti agenti approvati per l’uso negli Stati Uniti sono noti trigger di MH: anestetici generali inalati, alotano, desflurano, enflurano, etere, isoflurano, sevoflurano e succinilcolina.,9 Sebbene i potenti anestetici per inalazione siano i principali fattori scatenanti, vi è una forte evidenza che gli agenti moderni possono causare reazioni MH nello stesso modo in cui l’alotano fa, in alcuni casi con reazioni a insorgenza ritardata che si verificano diverse ore in anestesia.10
La stragrande maggioranza dei casi di MH si sono verificati mentre un paziente stava ricevendo un agente anestetico volatile con o senza succinilcolina.,6 MH è stato riportato dopo la somministrazione di succinilcolina in assenza di agenti anestetici inalati; la maggior parte di questi casi erano in pazienti la cui suscettibilità MH è stata dimostrata mediante biopsia.11
MH è stato anche riportato in individui MH-suscettibili dopo l’esposizione a stress da calore o esercizio fisico vigoroso. Sono stati riportati rari casi di bambini che sviluppano MH fatale spontanea in condizioni di vita normali, con test post mortem che rivelano mutazioni anormali del recettore della ryanodina.,12,13
Presentazione
MH può verificarsi in sala operatoria o subito dopo, nel periodo postoperatorio iniziale. La presentazione di MH varia e la maggior parte dei pazienti non sviluppa tutti i segni. In una revisione di 255 eventi MH, l’ordine di comparsa dei segni clinici, dal primo al più recente, era il seguente: spasmo massetere, ipercarbia, tachicardia sinusale, rigidità muscolare, tachipnea, cianosi, screziature cutanee, temperatura in rapido aumento, temperatura elevata, sudorazione, tachicardia ventricolare, urina color cola, fibrillazione ventricolare e sanguinamento eccessivo.,6
La presentazione di pazienti pediatrici con MH acuta varia in base all’età. Secondo il Registro di ipertermia maligna del Nord America, tachicardia sinusale, ipercarbia e rapido aumento della temperatura erano i segni più comuni di MH acuta nei pazienti di 18 anni e più giovani; questi risultati erano anche più comuni nei pazienti di età compresa tra 13 e 18 anni (coorte più antica). I bambini di età compresa tra 25 mesi e 12 anni (coorte media) hanno avuto più spasmo massetere e quelli di età compresa tra 0 e 24 mesi (coorte più giovane) hanno avuto maggiori probabilità di sviluppare screziature cutanee e la metà delle probabilità di sviluppare rigidità muscolare.,14
È un equivoco che l’ipertermia sia il segno iniziale di presentazione di MH. L’ipertermia si presenta tipicamente più successivamente ed è assente quando la circostanza in primo luogo è sospettata. Nella revisione di 255 casi di MH, l’ipertermia è stata uno dei primi segni in appena l ‘ 8,2% delle crisi ed è stata l’unico segno iniziale nel 3,9%.6 Le reazioni fulminanti MH sono rare; la maggior parte dei casi sono più lente e mostrano sottili cambiamenti. Il MHAUS gestisce una hotline di 24 ore che può essere consultato per l’assistenza di emergenza.,
Trattamento
Le indicazioni per il trattamento di MH comprendono segni di ipermetabolismo, rapido aumento dell’anidride carbonica (l’acidosi metabolica può essere ritardata), tachicardia e rigidità muscolare o mascellare. I pazienti potrebbero non presentare tutti questi segni clinici, ma senza una diagnosi alternativa persuasiva, si raccomanda di iniziare dantrolene e interrompere immediatamente gli agenti scatenanti piuttosto che aspettare troppo a lungo per farlo, il che potrebbe portare a un esito negativo.,1
Secondo l’MHAUS, queste quattro cose dovrebbero essere fatte il prima possibile nel trattamento di un evento MH acuto15:
1. Informare il chirurgo di terminare la procedura non appena possibile e interrompere gli agenti volatili e la succinilcolina.
2. Ottenere il dantrolene / MH carrello; se in un centro chirurgico piuttosto che un ospedale, chiamare il 911.
3. Iperventilare il paziente con ossigeno al 100% a 10 L/minuto.
4. Somministrare dantrolene.
IV dantrolene è l’unico farmaco approvato dalla FDA per il trattamento di MH., Il dantrolene è un rilassante muscolare scheletrico derivato dall’idantoina che agisce interferendo direttamente con il rilascio di calcio dal reticolo sarcoplasmatico. L’evidenza suggerisce che, durante una reazione MH, gli agenti scatenanti producono un cambiamento nelle cellule muscolo-scheletriche del paziente, con conseguente aumento del calcio mioplasmatico; si pensa che il dantrolene prevenga o riduca questo aumento, che attiva i processi catabolici acuti associati a MH.16 Dantrolene è una soluzione isotonica con un’emivita di 4-11 ore. La dose iniziale raccomandata dal MHAUS è 2.,5 mg / kg, con la dose ripetuta continuamente fino a quando i sintomi non diminuiscono; in alcuni pazienti possono essere necessarie dosi elevate (>10 mg/kg) e si suggerisce di prendere in considerazione una diagnosi alternativa se grandi dosi di dantrolene non risolvono i sintomi.
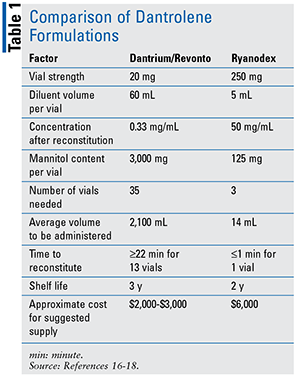
Ci sono due formulazioni disponibili di dantrolene. Dantrium e Revonto, la formulazione più vecchia, forniscono 20 mg di dantrolene sodico / 60 mL dopo ricostituzione in acqua sterile., Dantrium e Revonto devono essere ricostituiti aggiungendo 60 mL di Acqua sterile per preparazioni iniettabili (senza agente batteriostatico) e il flaconcino deve essere agitato fino a quando la soluzione non è limpida. La formulazione più recente, Ryanodex, è una sospensione iniettabile di dantrolene sodico che fornisce 250 mg di dantrolene sodico / 5 mL dopo ricostituzione. Ogni flaconcino di Ryanodex deve essere ricostituito con 5 ml di Acqua sterile per preparazioni iniettabili (senza agente batteriostatico) e agitato per garantire una sospensione uniforme, opaca, di colore arancione. Vedere la TABELLA 1 per un confronto delle formulazioni di dantrolene.,16-18
si raccomanda di gas del sangue essere sottoposti a test per determinare il grado di acidosi metabolica, e il provider dovrebbe prendere in considerazione la somministrazione di bicarbonato di sodio ad un dosaggio di 1 a 2 mEq/kg per un eccesso di base superiore a -8, per un dosaggio massimo di 50 mEq. I pazienti con MH devono essere raffreddati se la loro temperatura interna è superiore a 39 ° C o sta rapidamente aumentando; il raffreddamento deve essere interrotto quando la temperatura è inferiore a 38°C., Patients with hyperkalemia should be treated with calcium chloride 10 mg/kg (maximum dose 2,000 mg) or calcium gluconate (maximum dose 3,000 mg), sodium bicarbonate 1 to 2 mEq/kg IV (maximum dose 50 mEq), glucose, and insulin (pediatric patients, 0.1 U regular insulin/kg IV and 0.5 g/kg dextrose; adult patients, 10 U regular insulin IV and 50 mL 50% dextrose), and glucose levels should be checked hourly. In the case of refractory hyperkalemia, albuterol, kayexelate, dialysis, or extracorporeal membrane oxygenation should be considered if a patient has experienced cardiac arrest.,15
Le disritmie devono essere trattate con farmaci standard; tuttavia, i bloccanti dei canali del calcio devono essere evitati durante una crisi MH perché possono peggiorare l’iperkaliemia e l’ipotensione. I pazienti che hanno una reazione MH devono essere diuresi a una produzione di urina superiore a 1 ml/kg/ora; se la creatin chinasi (CK) o il potassio aumentano, si deve sospettare la mioglobinuria e si deve iniziare un’infusione di bicarbonato di 1 mEq/kg/ora per alcalinizzare l’urina. È importante monitorare in modo appropriato i pazienti che manifestano una reazione MH, incluso il monitoraggio della temperatura interna e della produzione di urina.,15
Una volta che la reazione MH iniziale è sotto controllo e il paziente è stabile, il paziente deve essere continuamente monitorato in un’unità di cura post anestesia o in terapia intensiva per almeno 24 ore.17 Indicazioni che un paziente si sta stabilizzando sono livelli di anidride carbonica normali o in calo alla fine delle maree, frequenza cardiaca diminuita o stabile senza segni di aritmia, ipertermia risolutiva e rigidità muscolare generalizzata.,15 Immediatamente dopo una reazione acuta MH, il dantrolene deve essere continuato per almeno 24 ore alla dose di 1 mg/kg per iniezione endovenosa ogni 4-6 ore o per infusione endovenosa alla dose di 0,25 mg/kg/ora.15-18 Il MHAUS suggerisce che dantrolene può essere interrotto o l’intervallo di dosaggio aumentato fino a ogni 12 ore se tutti i seguenti criteri sono soddisfatti: stabilità metabolica per 24 ore, temperatura interna inferiore a 38°C, diminuzione di CK, nessuna evidenza di mioglobinuria e nessuna rigidità muscolare., È importante che i fornitori monitorino continuamente i pazienti per le complicanze correlate all’MH, che includono cambiamenti nella coscienza, aritmie cardiache e/o disfunzioni, edema polmonare, disfunzione renale secondaria a necrosi tubulare acuta, DIC, disfunzione epatica, debolezza muscolare (rabdomiolisi contro effetto del dantrolene) e sindrome compartimentale secondaria alla rabdomiolisi.15
Preparazione e prontezza
È importante che gli ospedali rispondano in modo appropriato ai casi di MH., I Centers for Medicare and Medicaid Services (CMS) hanno pubblicato i dati nel 2016 mostrando che, dal 2011 al 2015, le ispezioni in otto ospedali e sistemi sanitari hanno rivelato carenze legate alla preparazione MH. Problemi comuni MH-correlati incontrati dai sistemi sanitari sono 1) insufficiente fornitura di dantrolene e 2) personale non adeguatamente addestrato nella sua amministrazione.,19
Il MHAUS raccomanda che il dantrolene sia accessibile entro 10 minuti dalla decisione di trattare e che almeno 700 mg—sufficienti per trattare un paziente di 70 kg-siano disponibili; ciò equivale a 35 flaconcini da 20 mg o tre flaconcini da 250 mg. Il MHAUS suggerisce anche di conservare, in o vicino alla sala operatoria, un carrello MH contenente i farmaci necessari per il trattamento MH: dantrolene; Acqua sterile per preparazioni iniettabili; cinque flaconcini da 50 ml di bicarbonato di sodio (8.,4%); due flaconcini da 50 mL di destrosio 50%; due flaconcini da 10 mL di cloruro di calcio (10%); un flaconcino di insulina regolare 100 U/mL; tre siringhe preriempite di lidocaina per iniezione (2%) 100 mg/5 mL o 100 mg/10 mL; e un minimo di 3.000 mL di soluzione salina refrigerata. Si raccomanda inoltre che il carrello MH contenga tutte le attrezzature generali necessarie, apparecchiature di monitoraggio, forniture per l’assistenza infermieristica e forniture per test di laboratorio.,20 Il CMS non fornisce una politica dettagliata su come le organizzazioni sanitarie saranno esaminate sulla loro capacità di rispondere a una crisi MH, ma si aspetta che seguano gli attuali standard di pratica, che sono delineati dal MHAUS.19
Conclusione
Sebbene MH sia un evento raro che complica solo circa uno su 100.000 interventi chirurgici, può essere mortale. Gli individui MH-suscettibili spesso non sanno di essere suscettibili fino a quando non si verifica una reazione MH., Strutture sanitarie che utilizzano agenti che possono innescare MH-anestetici volatili e succinilcolina-devono essere pronti a rilevare rapidamente e iniziare il trattamento per MH. MH può verificarsi in sala operatoria o poco dopo. La presentazione di MH può variare e molti pazienti non sviluppano tutti i segni. È un equivoco che l’ipertermia sia il segno iniziale di presentazione; in genere si verifica in seguito e quindi non è presente quando MH viene diagnosticata per la prima volta., Una volta che si sospetta un evento MH, il chirurgo deve essere avvisato di interrompere immediatamente la procedura e interrompere anestetici volatili e succinilcolina. Il paziente deve essere iperventilato con ossigeno al 100% a 10 L/minuto e dantrolene somministrato il prima possibile. È imperativo che il personale che risponderà a una reazione MH abbia familiarità con il sito Web MHAUS e i suoi contenuti per garantire che il loro team sia adeguatamente addestrato e che la loro struttura abbia le modalità di trattamento raccomandate prontamente disponibili al fine di ottenere il miglior risultato possibile.
Leave a Reply