| Formic acid | |
|---|---|
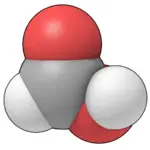 |
|
| General | |
| Systematic name | Methanoic acid |
| Other names | Hydrogen carboxylic acid Formylic acid Aminic acid |
| Molecular formula | CH2O2 HCOOH |
| SMILES | O=CO |
| Molar mass | 46.,0254 g/mol |
| Appearance | Colorless, fuming liquid |
| CAS number | |
| Properties | |
| Density and phase | 1.22 g/mL, liquid |
| Solubility in water | Miscible |
| Other solvents | Ethanol, acetone, ether |
| Melting point | 8.4°C (47.1°F) |
| Boiling point | 100.8°C (213.3°F) |
| Acidity (pKa) | 3.75 |
| Viscosity | 1.,57 cP at 26°C |
| Structure | |
| Molecular shape | Planar |
| Dipole moment | 1.41 D(gas) |
| Hazards | |
| MSDS | ScienceLab.com |
| Main hazards | Corrosive; irritant; sensitizer.,68693″> 2
3
0
|
| Flash point | 69°C (156°F) |
| R-phrases | R10, R35 |
| S-phrases | S1/2, S23, S26, S45 |
| RTECS number | LQ4900000 |
| Supplementary data page | |
| Structure & properties | n, εr, etc.,haviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related carboxylic acids | Acetic acid Propionic acid |
| Related compounds | Formaldehyde Methanol |
| Except where noted otherwise, data are given for materials in their standard state (at 25°C, 100 kPa) |
|
Formic acid (systematic name methanoic acid) is the simplest carboxylic acid., Sen kaava on HCOOH tai CH2O2. Luonnossa sitä esiintyy monien Hymenoptera-lahkon hyönteisten, erityisesti muurahaisten pistoissa ja puremissa. Tällä hetkellä sitä käytetään säilöntäaineena karjan rehun, välituotteena kemianteollisuudessa synteettisiä prosesseja, ja koska aktiivinen ainesosa joissakin kotitalouksien kalkkia poistoaineet. Se on myös merkittävä palamisen tuote vapautuu ajoneuvot käynnissä metanoli sekoittaa bensiiniä. Muurahaishapon suolaa tai esteriä kutsutaan formaatiksi tai metanoaatiksi. Formaatti-ionilla on kaava HCOO−.
tätä happoa on käsiteltävä varoen., Kosketukseen nesteen kanssa muurahaishappoa tai sen keskittynyt höyryt voivat ärsyttää ja vaurioittaa ihoa, silmiä ja hengitysteitä.
Historia ja etymologia
jo viidestoista luvulla, jotkut alkemistien ja luonnontieteilijät olivat tietoisia siitä, että muurahainen mäkiä antoi pois happamassa höyry. Vuonna 1671, englanti luonnontieteilijä John Ray tuli ensimmäinen henkilö kuvaamaan eristäminen muurahaishappo tislaamalla suuri määrä muurahaisia. Nämä hyönteiset erittävät ainetta hyökkäys-ja puolustustarkoituksiin. Näin nimi ”muurahaishappo” keksittiin latinan antia tarkoittavasta sanasta formica.,
muurahaishappoa syntetisoi ensimmäisenä hydrosyaanihaposta ranskalainen kemisti Joseph Gay-Lussac. Vuonna 1855 toinen ranskalainen kemisti Marcellin Berthelot kehitti hiilimonoksidista synteesin, joka oli samanlainen kuin nykyään.
kemianteollisuudessa muurahaishappoa pidettiin pitkään vähämerkityksisenä yhdisteenä. 1960-luvun lopulla siitä tuli kuitenkin merkittäviä määriä etikkahapon tuotannon sivutuotteena. Sitä käytetään nykyään yhä enemmän säilöntäaineena ja antibakteerisena aineena karjanrehussa.,
ominaisuudet
muurahaishappo sekoittuu veteen ja useimpiin polaarisiin orgaanisiin liuottimiin ja liukenee jonkin verran hiilivetyihin. Useimmat yksinkertaiset formaattisuolat liukenevat veteen.
Kun liuotetaan hiilivedyt ja kun höyry-vaihe, muurahaishappo koostuu vety-ja vapaakauppa-dimeerit (paria molekyylejä) eikä yksittäisiä molekyylejä. Kaasufaasissa tämä vetysidos johtaa vakaviin poikkeamiin ideaalikaasulaista. Neste ja kiinteä valtiot, tämä happo koostuu verkko-vety-sidottu molekyylejä., Kuumennettaessa muurahaishappo hajoaa hiilimonoksidiksi ja vedeksi.
muurahaishapolla on suurin osa muiden karboksyylihappojen kemiallisista ominaisuuksista, mutta sillä on myös useita ainutlaatuisia ominaisuuksia. Esimerkiksi normaaliolosuhteissa se ei muodosta asyylikloridia eikä happoanhydridiä. Aivan viime aikoihin asti kaikki yritykset muodostaa jompaakumpaa näistä johdannaisista johtivat sen sijaan hiilimonoksidiin. Nyt on osoitettu, että anhydridiä voidaan valmistaa formyylifluoridin ja natriumformiaatin välisellä reaktiolla -78°C: ssa., Kloridi voi olla valmistettu kulkee HCl-liuos, 1-formimidazole vuonna monochloromethane klo -60°C. lisäksi muurahaishappoa osakkeita joitakin vähentävät ominaisuudet aldehydejä.
Muurahaishappo on ainutlaatuinen karboksyylihapot sen kyky osallistua lisäksi reaktiot alkeenit, tuottaa formaatti esterit. Läsnäollessa tiettyjä happoja, kuten rikkihappoa ja fluorivetyhappo, kuitenkin, toinen reaktio (variantti Koch reaktio) tapahtuu, jossa muurahaishappo lisää alkeeni tuottaa suuremman karboksyylihappo.,
Tuotanto
merkittävä määrä muurahaishappoa saadaan sivutuotteena valmistettaessa muita kemikaaleja, etenkin etikkahappoa. Koska tämä tuotantoreitti ei riitä vastaamaan nykyiseen kysyntään, jonkin verran muurahaishappoa on tuotettava sen itsensä vuoksi.
kun metanolia ja hiilimonoksidia yhdistetään vahvan emäksen läsnä ollessa, tuote on metyyliformiaatti, muurahaishapon esteri. Kemiallinen yhtälö voidaan kirjoittaa seuraavasti:
CH3OH + CO → HCOOCH3
teollisuuden, tämä reaktio suoritetaan nestemäisenä korkeassa paineessa., Tyypillisiä reaktioolosuhteita ovat 80°C: n ja 40 atmosfäärin paine. Käytetyin emäs on natriummetoksidi. Hydrolyysi metyyli-formaatti tuottaa muurahaishappoa:
HCOOCH3 + H2O → HCOOH + CH3OH
Suora hydrolyysi metyyli-formaatti vaatii runsaasti ylimääräistä vettä edetä tehokkaasti, ja jotkut tuottajat käyttävät epäsuoraa reittiä.
laboratoriossa muurahaishappoa saadaan kuumentamalla oksaalihappoa vedettömässä glyserolissa, uuttamalla tuote höyrytislauksella., Toinen valmistelu (joka on suoritettava vetokaapissa) on happo hydrolyysi etyyli isonitrile käyttämällä suolahappoa.
C2H5NC + 2H2O → C2H5NH2 + HCOOH
Käyttää
pääasiallinen käyttö muurahaishappo on säilöntäaineena ja antibakteerinen agentti karjan rehuksi. Kun ruiskutetaan tuoretta heinää tai muita säilörehun, se pidätyksiä tiettyjä prosesseja rappeutuminen ja aiheuttaa rehun säilyttää ravintoarvo enää, ja niin se on laajalti käytetty säilyttää talvella rehua karjaa varten. Siipikarjateollisuudessa sitä lisätään joskus rehuun salmonellabakteerien tappamiseksi.,
lisäkäyttöä:
- sitä käytetään orgaanisen lateksin (sap) jalostamiseen raakakumiksi.
- mehiläishoitajat käyttävät muurahaishappoa märkänä Varroapunkkia vastaan.
- sillä on vähäinen merkitys tekstiiliteollisuudessa ja nahan parkitsemisessa.
- jotkut formaattiesterit ovat keinotekoisia aromeja tai hajuvesiä.
- se on vaikuttava aine eräillä kotitalouksien limescale remover-tuotemerkeillä.
- Sitä käytetään laboratorioissa liuottimena muokkaaja HPLC erotteluja proteiineja ja peptidejä, varsinkin kun näyte on valmis massaspektrometria analyysi.,
- synteettinen orgaaninen kemia, muurahaishappoa käytetään usein lähteenä hydride-ioni (jonka Eschweiler-Clarke reaktio tai Leuckart-Wallach reaktio) ja lähteenä vedyn mitä kutsutaan ”siirto hydraus.”
- laboratoriossa hiilimonoksidin lähteenä käytetään muurahaishappoa, jota vapautuu lisäämällä rikkihappoa. Se on myös formyyliryhmän lähde reaktiossa, joka tunnetaan nimellä ” formylaatio.,”
Turvallisuus
pääasiallinen vaara muurahaishappo on iho-tai silmäkosketus nestemäisellä muurahaishapolla tai keskittynyt höyryjä. Kaikki nämä altistumisreitit voi aiheuttaa vakavia kemiallisia palovammoja, ja silmien altistuminen voi aiheuttaa pysyviä silmävaurioita. Hengitettävät höyryt voivat myös aiheuttaa ärsytystä tai palovammoja hengitysteissä. Koska hiilimonoksidia voi esiintyä myös muurahaishappohöyryissä, on syytä olla varovainen, jos muurahaishappohöyryjä on suuria määriä. Yhdysvallat., OSHA sallittu altistustaso (PEL) muurahaishappohöyryn työympäristössä on viisi osaa miljoonaa osaa ilmaa (ppm).
muurahaishappo metaboloituu helposti ja eliminoituu elimistöstä. Joitakin kroonisia vaikutuksia on kuitenkin dokumentoitu. Jotkut eläinkokeet ovat osoittaneet sen olevan mutageeni, ja krooninen altistuminen voi aiheuttaa maksa-tai munuaisvaurioita. Toinen mahdollisuus krooniseen altistukseen on ihoallergian kehittyminen, joka ilmenee uudelleen altistumisesta kemikaalille.
muurahaishapon liuosten vaarat riippuvat pitoisuudesta.,ety symbol
| Concentration by weight |
Classification | R-Phrases |
|---|---|---|
| two to ten percent | Irritant (Xi) | R36/38 |
| 10–90 percent | Corrosive (C) | R34 |
| >90 percent | Corrosive (C) | R35 |
See also
- Acetic acid
- Acid
- Carboxylic acid
Notes
- Julius B., Cohen, Practical Organic Chemistry (MacMillan, 1930).
- isonitriili saadaan reagoimalla etyyliamiini kloroformin kanssa. Savuhuppua tarvitaan isonitriilin yliherkän vastenmielisen hajun vuoksi.
- L. F. Fieser ja J. E. Jones, ”N-methylformanilide” Orgaaniset Synteesit Coll. Vol. 3 (1955): 590; 20(1940): 66. Viitattu 31.12.2007.
kaikki linkit haettu 19.huhtikuuta 2017.,
- NIOSH Pocket Guide to Kemialliset Vaarat: Muurahaishappo
– Hyvitykset
New World Encyclopedia kirjailijat ja toimittajat rewrote ja valmistunut Wikipedia articlein mukaisesti New World Encyclopedia standardeja. Tämä artikkeli noudattaa ehtojen Creative Commons CC-by-sa 3.0-Lisenssin (CC-by-sa), joita voidaan käyttää ja levittää kunnon nimeä. Luotto erääntyy alle tämän lisenssin ehtoja, jotka voivat viitata sekä New World Encyclopedia avustajat ja epäitsekäs vapaaehtoisia tukijoita Wikimedia Foundation., Voit lainata tämän artikkelin klikkaa tästä luettelo hyväksyttävistä vedoten muodoissa.Historian aiemmin maksut by wikipedian käyttäjiä on kaikkien tutkijoiden täältä:
- Muurahaishappo historia
historia tämä artikkeli, koska se oli tuotu New World Encyclopedia:
- Historia ”Muurahaishappo”
Huomautus: Joitakin rajoituksia voidaan soveltaa, käyttää yksittäisiä kuvia, jotka on erikseen lisensoitu.
Leave a Reply