 organisk kjemi kurset vil dekke mange forskjellige typer av isomerene.
organisk kjemi kurset vil dekke mange forskjellige typer av isomerene.
Isomerene har samme molekylær formel, men noe om dem er forskjellige.
Geometriske isomere former, en type stereoisomer, ulik geometri og form. Dette skjer når substituenter er LÅST i et bestemt forhold til hverandre.,
jeg si låst fordi, i motsetning til conformational isomerene i Newman Anslag, du kan ikke bare vri-molekylet for å endre forholdet mellom substituenter.
I denne opplæringen vil vi se på alken geometriske isomere former, inkludert cis-trans-og E Z.
Cis/Trans Isomerism
Cis/Trans isomerism er vanligvis sett med substituenter på hver side av alken dobbeltbindingen.
Hvordan skjer dette?
Alken dobbeltbindinger oppstå mellom sp2 hybridiserte karbon atomer. Husker: sp2 hybrider har en trigonal-plan eller «flatt» geometri.
(Ikke komfortabel med dette?, Gjennomgang sp2 Hybridisering.)
Men det er ikke hybrid vi ser på.
i Stedet, det er fn-hybridiserte p-orbital som danner en ANDRE bånd mellom de 2 c-atomer.
En sp3 hybridiserte enkelt-eller simga bond er gratis å rotere.
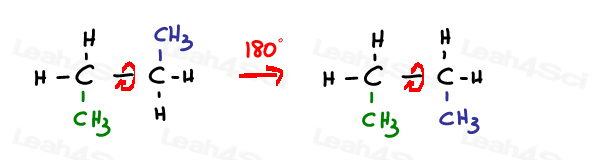
Sp2 pi obligasjoner er låst på plass.
Den eneste måten å rotere denne bindingen er å bryte dobbeltbindingen, rotere, – og administrasjonsdepartementet dobbeltbindingen –som vanligvis er ikke observert.
faktisk, dette krever høy energi, som du vil se i din Diels Alder reaksjoner senere.,
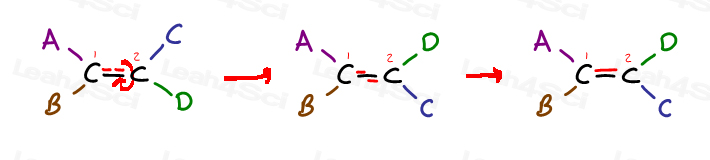
Ta en titt på følgende generisk alken og det er 4 substituenter:
Carbon 1 har substituenter A og B; Carbon 2 har substituenter C og D.
Men legg merke til at spesielt hvordan En er på samme side som C, og B er på samme side som D.
Den eneste måten å få En ved siden D er å bryte pi bond, rotere molekyl, – og administrasjonsdepartementet pi bond. Ellers er låst på plass i nærheten av C og B er låst på plass nærheten D.,
Cis vs Trans mellom hx og alkener
La oss ta en titt på 2 versjoner av 2-butene: 2-butene er et 4-karbon kjede med et dobbelt bånd mellom karbonatomer 2 og 3.
Så, kan vi trekke dette på feil måte, som et lineært molekyl:
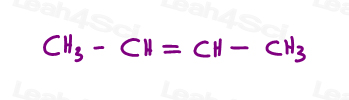
Eller, draw hver sp2 karbon i en 120 graders bond vinkel. Dette gir meg muligheten til å plassere både metyl-grupper på opp, ned, eller en opp og en ned.
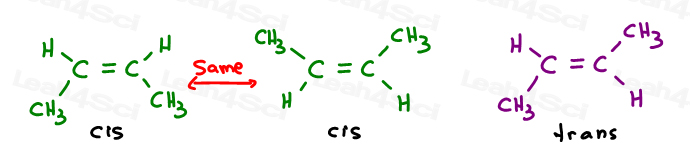
De to første er faktisk det samme: både cis., Du skjønner, jeg kan snu molekylet, og gjør de første overlappe (overlapp) den andre uten å bryte noen obligasjoner.
Den tredje er unik. Den eneste måten å legge det tredje er å bryte dobbeltbindingen.
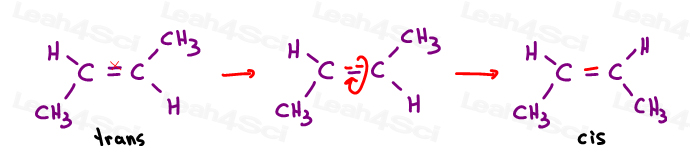
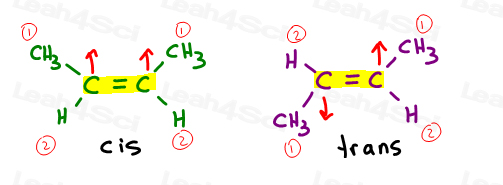
Cis mellom hx og alkener
jeg liker å tenke på cis som «søstre». De er sammen på samme side.
Cis mellom hx og alkener har substituenter på samme side av dobbeltbindingen.
Trans mellom hx og alkener
jeg liker å tenke på trans substituenter som å ha » overføres adskilt fra hverandre.’Å sette dem på motsatte sider.,
Trans mellom hx og alkener har sine substituenter på motsatte sider.
Navngi Cis/Trans mellom hx og alkener:
Når du har identifisert cis/trans mellom hx og alkener, navngi dem er ganske enkel.
1) Første navnet alken ved hjelp av opplæringen knyttet nedenfor.
2) Deretter kan du enkelt legge til ‘cis’ eller ‘overs’ foran navnet.,
Ta 2 geometriske isomere former av 2-butene:
Sine riktige navn er som følger:
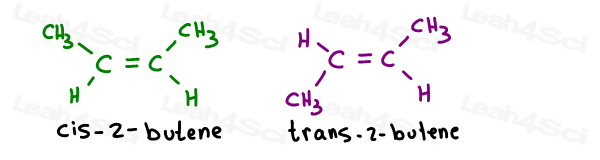
Når det er bare en pi bond, trenger du ikke å angi hvilke karbon er cis-eller trans siden. Det er selv-forstått.
Når du har mer enn én dobbeltbindingen på molekylet, må du angi hvilken er cis-og trans.,
Ta dette molekylet for eksempel: 2,5-octadiene

Dette molekylet har 2 pi obligasjoner. En cis og ett overs.
Siden det er mer enn én pi bond, må du angi hvilken pi bond er cis-og trans.
Alken stabilitet
Ikke alle isomerene har samme stabilitet.
Det handler om stabilitet – i organisk kjemi eller vitenskap generelt.

Trans mellom hx og alkener er MER STABIL enn cis kolleger.,
Dette er mer tydelig med større substituenter.
Trans mellom hx og alkener
I en trans alken, substituenter er vendt bort fra hverandre.
De ikke «få i hverandres ansikter» og derfor ikke har noe i de andre gruppene.
Cis mellom hx og alkener
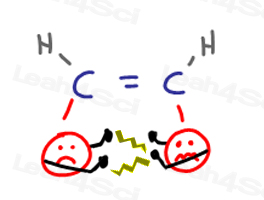 Cis alken substituenter er tett sammen, og vil » komme i hverandres ansikter.’Dette fører til ‘argumenter» når en gruppe invaderer andres personlige plass.
Cis alken substituenter er tett sammen, og vil » komme i hverandres ansikter.’Dette fører til ‘argumenter» når en gruppe invaderer andres personlige plass.
Når gruppene prøver å bevege seg bort fra hverandre, kan de forårsake press på molekylet.,
Alt dette fører til en ulykkelig og høyere energi cis konformasjon.
Cis & Trans på Sykliske Forbindelser
Ring strukturer eller sykliske forbindelser kan også vise cis/trans isomerism uten tilstedeværelse av en pi bond.
Husk, substituenter vil være cis-og trans hvis de er låst på plass. Pi obligasjoner er en måte å låse dem på plass. Ringene er en annen sak.
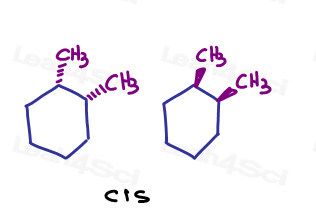
For eksempel, i 1,2-dimethylcyclohexane, jeg kan vise både substituenter går inn i siden eller begge går ut av siden.,
Siden de peker i samme retning, de er cis til hverandre.
Hvis jeg vise en kommer inn på siden, og man kommer ut på siden. De er overs til hverandre.
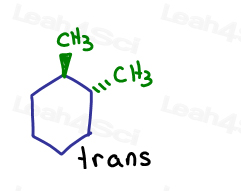
Selv om karbonatomer er sp3 og sigma bundet til hverandre, molekylet selv ikke kan rotere på grunn av ringen struktur. Låse.
Den eneste måten å slå cis-1,2-dimethylcyclohexane i trans-1,2-dimethylcyclohexane, er å bryte åpne ringen, rotere, – og administrasjonsdepartementet ringen.,
Hva om det er mer enn en substituent på sp2 karbon?
Til nå har vi sett på molekyler med bare en substituent på hver side av sp2 pi bundet karbon.
Hva skjer hvis vi har en pi-bånd med 2 forskjellige atomer eller grupper på sp2 karbon?
Ta en titt på 3-methyl-2-pentene:
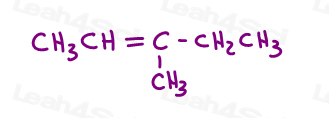
Her i linje struktur:
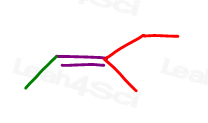
Du kan tegne dette molekylet i 2 forskjellige måter. Men vil du sammenligne den røde methyl eller rød ethyl til den grønne methyl når du velger cis eller overs?,
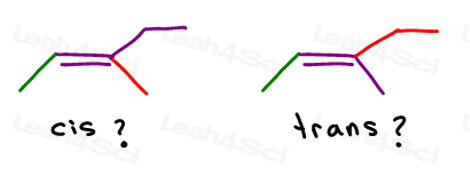
Mens noen professorer VIL lære deg å sammenligne større grupper, svaret er at du IKKE kan sammenligne rett og slett velge en for cis-og trans.
Innføre E Z Notasjonen
Når en pi bond har mer enn en substituent på hver side, eller som inneholder ikke-karbon substituenter, vi trenger et mer avansert system for å identifisere geometriske isomerism.
E Z systemet krever rangering av grupper på hver side av pi bond., Vi må finne ut om høyere prioriterte grupper er ved siden av hverandre, Z (tror cis), eller er borte fra hverandre, E (tror overs).
Men først må vi lære hvordan å rangere grupper som bruker Cahn-Ingold-Prelog notasjon.
videoen under er fra min chirality serien, men lærer dette konseptet i detalj. Begynne å se fra 0:52
Cahn-Ingold-Prelog i oppsummering:
Vi er rangeringen atomer basert på sine atom-nummeret.
Ikke massen av gruppen, ikke størrelsen på gruppen.
Jo høyere atomnummer av atom direkte tilkoblet, jo høyere prioritet.,
Here are the 10 most common atoms you’ll come across from high to low priority:
I > Br > Cl > S > P > F > O > N > C > H
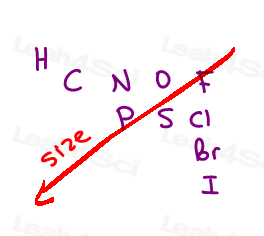
Here’s My Simple Approach
- Highlight your double bond, then look at just one half of the molecule at a time., Bruk din hånd eller annet papir for å dekke den andre halvparten av molekylet.
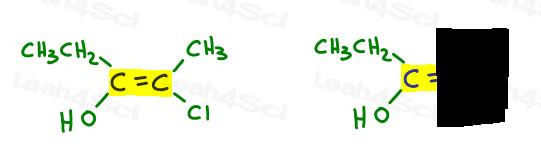
- Avgjøre hvilken gruppe som er høyere prioritert, og sette et nummer 1.
jeg liker å tegne en pil vinkelrett på pi bond så jeg kan tydelig se om det er opp eller ned ved sammenligningen.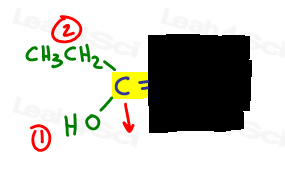
- Gjør det samme for den andre siden.,
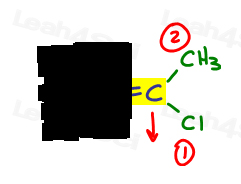
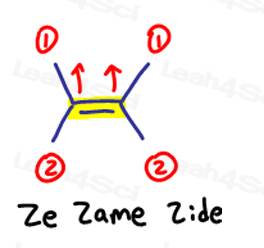
E er for Eeposite, Z er for Ze Zame Zide
Hvis de to høyt prioriterte grupper er motsatt til hverandre, tenker på dem som ‘eeposite» til hverandre.
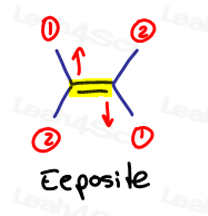 E er for Eeposite.
E er for Eeposite.
Hvis de to høyt prioriterte grupper er på samme side, eller skal jeg si på ‘Ze Zame Zide,’ de er Z.
Dette gjelder molekyler som har mer enn bare 1 karbon på hver side av dobbeltbindingen.
Ze Zame Zide.,
La oss gå tilbake til eksemplet over:
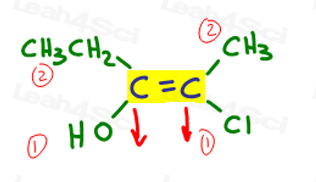
På venstre, OH outranks ethyl siden oksygen har høyere atomnummer i forhold til karbon. OH er #1 og peker nedover.
På høyre, Cl outranks methyl siden klor har en høyere atomnummer i forhold til karbon. Cl er #1 og peker nedover.
Siden begge pilene peker i samme retning (nedover), kan vi konkludere med at de prioriterte gruppene er på Ze Zame Zide gjør det Z.,
2 Lik Prioritet Grupper
noen Ganger vil du se en lure-spørsmål, hvor en sp2 karbon vil ha 2 av nøyaktig samme grupper.
Siden du kan ikke rangere en over den andre, vil det IKKE være cis/trans eller E/Z isomerism.
Her er 2 vanlige eksempler:
1) En terminal pi bond
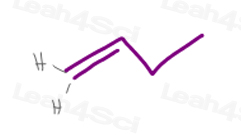
Karbon #1 i 1-butene har 2 hydrogenatomer.
Siden H v H har samme prioritet, dette molekylet har ingen cis/trans eller E/Z isomerism.,
2) nøyaktig Samme grupper på samme sp2 pi bundet karbon.

Karbon #2 i 2-methyl-2-butene har 2 CH3-grupper.
– En ser ut til å være en del av den overordnede kjeden, den andre ser ut til å være en methyl substituent.
Men, når CH3 er i forhold til CH3 rangerte de akkurat det samme.
Dette molekylet har ingen cis/trans n/eller E/Z isomerism.,
Cis-og Trans vs E og Z
Hvis vi går tilbake til våre cis/trans praksis problemer, slik som cis-og trans 2-butene, vil du se at vi kan bruke E/Z-systemet her også.
Carbon 2 og 3 har en methyl gruppe outranking et hydrogenatom. Når de er cis, får du Z. Når de er trans du får E.
Et ord av forsiktighet
Du KAN bruke E/Z for cis/trans isomerene, men du kan ikke bruke cis/trans for komplekse E/Z-isomerene som vi allerede har vist ovenfor.,
Oppsummering
Cis vs overs og E vs Z isomerene er geometriske isomere former som oppstår når substituenter er låst i posisjon ved siden av eller overfor hverandre. Dette er sett i både doble obligasjoner for mellom hx og alkener, og substituenter på ringen strukturer.
Cis mellom hx og alkener er på samme størrelse, trans mellom hx og alkener er på motsatte sider. Når substituenter er mer komplisert bruke de mer avanserte E/Z-notasjon etter å bestemme forholdet mellom høyt prioriterte grupper.
Leave a Reply