Podělte se o svůj názor + otevřené poznámky. Vypočítává se aktuální počet anotací na této stránce.
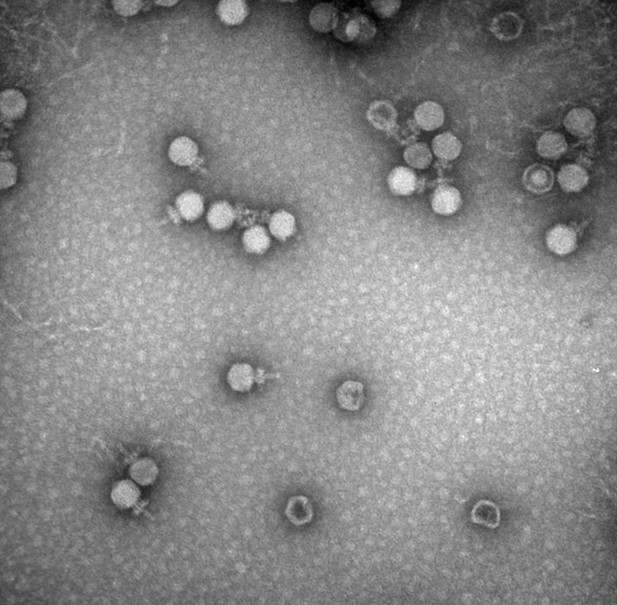
transmisní elektronová mikroskopie obrázek bakteriofágy přijata na University of Alabama Optické Analýzy Zařízení. Autor: Chou-Zheng a Hatoum-Aslan, 2019 (KC by 4.,0)
stejně jako lidé, jsou náchylné na viry, bakterie mají své vlastní viry potýkat. Tyto viry – známý jako bakteriofágy – připojit k povrchu bakteriální buňky, aplikovat jejich genetický materiál, a použít buněk, enzymů se množit, zatímco ničí jejich hostitelů.
k obraně proti fágovému útoku se bakterie vyvinuly v různých imunitních systémech., Například, když bakterie s imunitním systémem známým jako CRISPR-Cas narazí na fág, systém vytvoří „paměť“ útočníka zachycením malého úryvku genetického materiálu phage. Kousky fágové DNA jsou kopírovány do malých molekul známých jako CRISPR RNA, které se pak kombinují s jedním nebo více Cas proteiny a vytvářejí skupinu nazývanou komplex Cas. Tento komplex hlídá vnitřek buňky a nese CRISPR RNA pro srovnání, podobně jako detektiv používá otisk prstu k identifikaci zločince., Jakmile je nalezena shoda, proteiny Cas nasekají napadající genetický materiál a zničí fág.
existuje několik různých typů systémů CRISPR-Cas. Typ III systémy patří mezi nejvíce rozšířené v přírodě a jsou jedinečné v tom, že poskytují téměř neproniknutelnou bariéru pro fágů se snaží infikovat bakteriální buňky. Lékařští vědci zkoumají použití fágů jako alternativ ke konvenčním antibiotikům, a proto je důležité najít způsoby, jak překonat tyto imunitní odpovědi u bakterií., Zůstává však nejasné, jak přesně jsou systémy CRISPR-Cas typu III schopny takovou účinnou obranu namontovat.
Chou-Zheng a Hatoum-Aslan použili genetické a biochemické přístupy ke studiu systému CRISPR-Cas typu III v bakterii zvané Staphylococcus epidermidis. Experimenty ukázaly, že dva enzymy zvané PNPase a RNase J2 hrály klíčovou roli v obranné reakci vyvolané systémem. Pnpáza pomohla generovat CRISPR RNA a oba enzymy byly vyžadovány, aby pomohly zničit genetický materiál napadením fágů.,
předchozí studie ukázaly, že Pnpáza a Rnáza J2 jsou součástí stroje v bakteriálních buňkách, které obvykle degradují poškozený genetický materiál. Proto tato zjištění ukazují, že systém CRISPR-Cas typu III V s.epidermidis se vyvinul tak, aby koordinoval s jinou cestou, která pomáhá bakteriím přežít útok z fágů. Imunitní systémy CRISPR-Cas vytvořily základ pro celou řadu technologií, které i nadále revolucionizují genetiku a biomedicínský výzkum., Proto spolu s podporou hledání alternativ k antibiotikům může tato práce v budoucnu potenciálně inspirovat vývoj nových genetických technologií.
Leave a Reply