o núcleo de um átomo é circundado por elétrons que ocupam conchas, ou orbitais de diferentes níveis de energia.
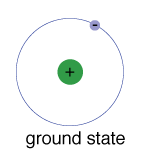
O estado fundamental de um elétron, o nível de energia é normallyoccupies, é o estado de menor energia para o elétron.
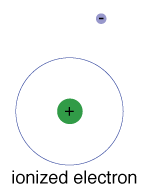
há também uma energia máxima que cada elétron pode ter e ainda fazer parte de seu átomo., Além dessa energia, o elétron não está mais ligado ao núcleo do átomo e é considerado ionizado.quando um elétron ocupa temporariamente um estado de energia maior que o seu estado no solo, ele está em um estado excitado. Um elétron pode ficar excitado se receber energia extra, como se absorvesse um fóton, ou pacote, de luz, ou colidisse com um átomo ou partícula próximos.
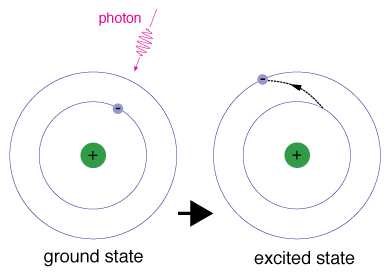
Cada orbital tem uma energia específica associada a ele., Para que o anelectron seja impulsionado para um orbital com uma energia mais elevada, ele deve obter a diferença de energia entre o orbital em que está, e o orbital para o qual está indo. Isto significa que ele deve absorver um fóton que contém precisamente essa quantidade de energia, ou tomar exatamente essa quantidade de energia de outra partícula em uma colisão.os elétrons não permanecem em estados excitados por muito tempo-eles retornam aos seus Estados terrestres, emitindo um fóton com a mesma energia que o que foi absorvido.,

as Transições entre os vários orbitais são únicos para cada elementbecause os níveis de energia são exclusivamente determinada por prótons andneutrons no núcleo. Quando os elétrons de um certo átomo retornam aos orbitais inferiores de estados excitados, os fótons que emitem têm energia que são características desse tipo de átomo. Isso dá a eachelement uma impressão digital única, tornando possível identificar os elementos presentes em um recipiente de gás, ou mesmo uma estrela.
atualizado: novembro de 2013
Leave a Reply