학습목표
- Arrhenius 산을 정의한다.
- Arrhenius 산의 예를 들어주십시오.
- hydronium 이온을 기술하십시오.
- Arrhenius 기초를 정의하십시오.
- Arrhenius 염기의 예를 들어주십시오.
Arrhenius Acids
너무 깊게 숨을 쉬지 마십시오.
 금성은 지구상 우리에게 가장 가까운,그러나 매우 다르고 적대적인 환경을 제공합니다.
금성은 지구상 우리에게 가장 가까운,그러나 매우 다르고 적대적인 환경을 제공합니다.
평균 약 450°C 의 표면 온도를 가지고 있습니다., 대기는 이산화탄소로 구성되어 있지만 황산의 구름은 상층 대기를 통해 이동하여 극도로 비우호적 인 조건을 조성하는 데 도움이됩니다. 이러한 조건 때문에 금성은 휴가에 방문하고 싶은 곳이 아닙니다.
산 계좌는 잔
스웨덴 화학 Svante 계좌는 잔(1859-1927)을 제안하는 첫번째이었 이론을 설명하는 관찰된 동작산 및니다. 전류를 전도하는 능력 때문에 그는 산과 염기 모두 용액에 이온을 함유하고 있음을 알고있었습니다., Arrhenius 산은 수용액에서 수소 이온(H+)을 산출하기 위하여 이온화하는 화합물입니다.
산은 이온화 가능한 수소 원자를 갖는 분자 화합물이다. 극성이 높은 공유 결합의 일부인 수소 원자 만 이온화 가능합니다. 염화수소(HCl)는 실온에서 정상 압력 하에서 가스입니다. 염화수소의 H-Cl 결합은 극성 결합이다. 수소 원자는 염소 원자의 전자 음성도가 높기 때문에 전자가 결핍되어있다., 물 물.결과적으로,수소 원자는 hcl 이 물에 용해 될 때 물 분자에서 전자의 고독한 쌍에 끌린다. 그 결과 H-Cl 결합이 끊어지고 두 결합 전자가 cl 과 함께 남아있어 염화물 이온이 형성됩니다. H+이온은 물 분자에 부착되어 hydronium 이온이라고 불리는 다 원자 이온을 형성합니다. Hydronium 이온(H3O+)은 수소 이온이 부착 된 물 분자로 생각할 수 있습니다.

그림 1. 하이드로 늄 이온의 형성.,
방정식을 보여주는 이온화의 산에서 물 자주 간체에 의해 생략하는 물 분자:
![]()
이것은 단순히 단순화 이전의 방정식,그러나 그것은 일반적으로 사용됩니다. 수용액 내의 임의의 수소 이온은 하이드로 늄 이온으로 물 분자에 부착 될 것이다.
 분자 화합물의 모든 수소 원자가 이온화 가능한 것은 아닙니다. 메탄(CH4)에서,수소 원자는 단지 약간 극성 인 결합에서 탄소에 공유 결합된다., 수소 원자는 이온화 할 수 없으며 메탄은 산성 특성이 없습니다. 아세트산(CH3COOH)은 유기산이라고 불리는 산의 부류에 속합니다. 분자에는 4 개의 수소 원자가 있지만 산소 원자에 결합 된 수소 하나만 이온화 가능합니다.
분자 화합물의 모든 수소 원자가 이온화 가능한 것은 아닙니다. 메탄(CH4)에서,수소 원자는 단지 약간 극성 인 결합에서 탄소에 공유 결합된다., 수소 원자는 이온화 할 수 없으며 메탄은 산성 특성이 없습니다. 아세트산(CH3COOH)은 유기산이라고 불리는 산의 부류에 속합니다. 분자에는 4 개의 수소 원자가 있지만 산소 원자에 결합 된 수소 하나만 이온화 가능합니다.
O-H 결합은 이온화되어 H+이온 및 아세테이트 이온을 수득할 수 있다. 이 분자의 다른 수소 원자는 산성이 아닙니다.,e common acids:
| Acid Name | Formula |
| Hydrochloric acid | HCl |
| Nitric acid | HNO 3 |
| Sulfuric acid | H 2 SO 4 |
| Phosphoric acid | H 3 PO 4 |
| Acetic acid | CH 3 COOH |
| Hypochlorous acid | HClO |
A monoprotic acid is an acid that contains only one ionizable hydrogen., 염산과 아세트산은 모노 프로틱 산입니다. 폴리 프로트 산은 여러 개의 이온화 가능한 수소를 포함하는 산입니다. 가장 일반적인 폴리 프로 틱 산은 diprotic(예:H2SO4)또는 triprotic(예:H3PO4)입니다.
Arrhenius 염기
이것은 무엇을 위해 사용될 수 있습니까?

수산화 나트륨은 다목적 화학 물질입니다. 그것은 막힌 배수구를 청소하는 것과 같은 평범한 목적으로 사용될 수 있습니다. 몇몇 상업적 제제는이 목적을 위해 수산화 나트륨을 함유하고있다. 그것은 또한 식품 가공 분야에 있는 다수 신청이 있습니다., 아이스크림은 NaOH 를 사용하여 두껍게 만듭니다. 올리브가 수산화 나트륨 및 기타 화학 물질을 함유 한 용액에 담그면 올리브가 검게 변합니다. 부드러운 프레즐은 식품에 수산화 나트륨을 도포하여 질기게 만듭니다. 이 화합물에서 널리 이용되는 합성의 플라스틱,에칭 알루미늄,대한 페인트 제거,그리고 채용에 dehorning 의 가축(경우에는 당신이 필요).
Arrhenius 염기
Arrhenius 염기는 수용액에서 수산화 이온(OH−)을 산출하기 위해 이온화하는 화합물이다., The Table below lists several of the more common bases:
| Base Name | Formula |
| Sodium hydroxide | NaOH |
| Potassium hydroxide | KOH |
| Magnesium hydroxide | Mg(OH) 2 |
| Calcium hydroxide | Ca(OH) 2 |
All of the bases listed in the table are solids at room temperature., 물 속에 용해되면,각각은 금속 양이온과 수산화 이온으로 해리된다.
![]()
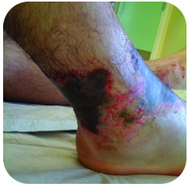
그림 2. 이 발은 잿물이라고도하는 수산화 나트륨 용액과의 장기간 접촉으로 인해 심한 화상을 입습니다.
수산화 나트륨은 잿물이라고도하는 매우 부식성 물질입니다. 잿물은 엄격한 청소기로 사용되며 비누 제조의 성분입니다. 노출이 심한 화상을 초래할 수 있으므로 수산화 나트륨과 같은 강염기에주의를 기울여야합니다(그림 2 참조).,
나트륨은 알칼리 금속이라고 불리는 원소 그룹에 속합니다. 알칼리성 용액은 기본 용액의 또 다른 이름입니다. 모든 알칼리 금속은 물 쉽게 반응하여 금속 수산화물 및 수소 가스를 생성합니다. 결과 솔루션은 기본입니다.
기초로 구성되는 알칼리 금속은 양이온 및 음이온 수산화 모두에 잘 녹 물. 그룹 2 금속(알칼리 토금속)의 화합물도 기본입니다. 그러나,이들 화합물은 일반적으로 물에만큼 용해되지 않는다., 따라서 이들 화합물에 대한 해리 반응은 평형 반응으로 나타난다.
이러한 상대적으로 불용성 수산화물들의 화합물에서 논의 컨텍스트의 용해도는 제품을 일정한![]() . 의 용해도 마그네슘 수산화 0.0084g 당 리터의 물 25°C. 기 때문에 그것의 가용성,마그네슘 수산화되지 않으로 위험한 수산화 나트륨., 실제로,수산화 마그네슘은 제산제 또는 온화한 완하제로 사용되는 마그네시아의 우유라고 불리는 제품의 활성 성분입니다.
. 의 용해도 마그네슘 수산화 0.0084g 당 리터의 물 25°C. 기 때문에 그것의 가용성,마그네슘 수산화되지 않으로 위험한 수산화 나트륨., 실제로,수산화 마그네슘은 제산제 또는 온화한 완하제로 사용되는 마그네시아의 우유라고 불리는 제품의 활성 성분입니다.
요약
- Arrhenius 산이 정의된다.
- Arrhenius 산의 예가 주어진다.
- Arrhenius 염기가 정의됩니다.
- Arrhenius 염기의 예가 주어진다.
연습
자료를 읽 아래의 링크에서 다음과 같은 질문에 대답:
http://dwb4.unl.edu/Chem/CHEM869R/CHEM869RLinks/www.nidlink.com/7Ejfromm/arrhenius.htm
- 무엇이었을 계좌는 잔의 첫 번째 과학적인 아이디어?
- 박사위원회는 그것에 대해 어떻게 생각 했습니까?,
- 그는이 아이디어를 위해 무엇을 얻었습니까?
- Arrhenius 산의 해리에 대한 일반 방정식을 작성하십시오.
검토
Arrhenius Acids
- Arrhenius acid 란 무엇입니까?
- hydronium 이온은 무엇입니까?
- H2SO4 는 모노 프로틱 또는 폴리 프로틱 산입니까?
Arrhenius 기지
- Arrhenius 기지 란 무엇입니까?
- Arrhenius 염기를 형성 할 하나의 반응은 무엇입니까?
- 알칼리 토류 염기는 매우 물성입니까?
Leave a Reply