cíle učení
- definovat Arrhenius acid.
- Uveďte příklady arrheniových kyselin.
- popište hydroniový ion.
- Definujte arrheniovu základnu.
- Uveďte příklady arrheniových základen.
Arrheniovy kyseliny
nedýchají příliš hluboce.
 Venuše je planeta nejblíže k nám, ale má velmi odlišné a nepřátelské prostředí.
Venuše je planeta nejblíže k nám, ale má velmi odlišné a nepřátelské prostředí.
má povrchovou teplotu, která je v průměru kolem 450°C., Atmosféra se skládá z oxidu uhličitého, ale mraky kyseliny sírové se pohybují horní atmosférou, což pomáhá vytvářet extrémně nepřátelské podmínky. Kvůli těmto podmínkám není Venuše místem, které chcete navštívit na dovolené.
Arrheniovy Kyseliny
švédský chemik Svante Arrhenius (1859-1927) byl první navrhnout teorii vysvětlit pozorované chování kyselin a zásad. Vzhledem k jejich schopnosti provádět proud věděl, že jak kyseliny, tak báze obsahují ionty v roztoku., Kyselina Arrhenius je sloučenina, která ionizuje, aby poskytla vodíkové ionty (H + ) ve vodném roztoku.
kyseliny jsou molekulární sloučeniny s ionizovatelnými atomy vodíku. Ionizovatelné jsou pouze atomy vodíku, které jsou součástí vysoce polární kovalentní vazby. Chlorovodík (HCl) je plyn při pokojové teplotě a za normálního tlaku. Vazba H-Cl v chlorovodíku je polární vazba. Atom vodíku je nedostatek elektronů kvůli vyšší elektronegativitě atomu chloru., V důsledku toho je atom vodíku přitahován k osamělému páru elektronů v molekule vody, když je HCl rozpuštěn ve vodě. Výsledkem je, že vazba H-Cl se zlomí, přičemž oba spojovací elektrony zůstávají s Cl a tvoří chloridový iont. Iont H + se váže na molekulu vody a vytváří polyatomický iont zvaný hydroniový iont. Hydroniový ion (H 3 o+) lze považovat za molekulu vody s připojeným vodíkovým iontem.

Obrázek 1. Tvorba hydroniového iontu.,
Rovnice ukazuje, ionizace kyseliny ve vodě jsou často zjednodušena vynecháním molekulu vody,
![]()
Toto je pouze zjednodušením předchozí rovnice, ale to je běžně používané. Jakékoli vodíkové ionty ve vodném roztoku budou připojeny k molekulám vody jako ionty hydronia.
 ne všechny atomy vodíku v molekulárních sloučeninách jsou ionizovatelné. V metanu (CH 4) jsou atomy vodíku kovalentně spojeny s uhlíkem v vazbách, které jsou jen mírně polární., Atomy vodíku nejsou schopny ionizovat a metan nemá kyselé vlastnosti. Kyselina octová (CH 3 COOH) patří do třídy kyselin nazývaných organické kyseliny. V molekule jsou čtyři atomy vodíku, ale pouze jeden vodík, který je spojen s atomem kyslíku, je ionizovatelný.
ne všechny atomy vodíku v molekulárních sloučeninách jsou ionizovatelné. V metanu (CH 4) jsou atomy vodíku kovalentně spojeny s uhlíkem v vazbách, které jsou jen mírně polární., Atomy vodíku nejsou schopny ionizovat a metan nemá kyselé vlastnosti. Kyselina octová (CH 3 COOH) patří do třídy kyselin nazývaných organické kyseliny. V molekule jsou čtyři atomy vodíku, ale pouze jeden vodík, který je spojen s atomem kyslíku, je ionizovatelný.
vazba O-H může být ionizována, aby se dosáhlo iontu H + a acetátového iontu. Ostatní atomy vodíku v této molekule nejsou kyselé.,e common acids:
| Acid Name | Formula |
| Hydrochloric acid | HCl |
| Nitric acid | HNO 3 |
| Sulfuric acid | H 2 SO 4 |
| Phosphoric acid | H 3 PO 4 |
| Acetic acid | CH 3 COOH |
| Hypochlorous acid | HClO |
A monoprotic acid is an acid that contains only one ionizable hydrogen., Kyselina chlorovodíková a kyselina octová jsou monoprotické kyseliny. Kyselina polyprotická je kyselina, která obsahuje více ionizovatelných hydrogenů. Nejběžnější polyprotické kyseliny jsou buď diprotické (jako je H 2 SO 4 ) nebo triprotické (jako je H 3 PO 4 ).
Arrheniovy báze
k čemu to lze použít?

hydroxid sodný je univerzální chemická látka. Může být použit pro takové světské účely, jako je čištění ucpaných odtoků. Několik komerčních přípravků obsahuje pro tento účel hydroxid sodný. Má také řadu aplikací v oblasti zpracování potravin., Zmrzlina je zesílena pomocí NaOH. Pokud jsou olivy namočené v roztoku obsahujícím hydroxid sodný a jiné chemikálie, olivy zčernou. Měkké preclíky jsou žvýkány aplikací hydroxidu sodného na potraviny. Tato sloučenina byla široce používána při syntéze plastů, pro leptání hliníku, pro odstraňování nátěrů a používá se při odstraňování skotu (v případě, že je to potřeba).
Arrheniovy Bází
báze podle arrhenia je sloučenina, která ionizuje výnos hydroxidových iontů (OH− ) ve vodném roztoku., The Table below lists several of the more common bases:
| Base Name | Formula |
| Sodium hydroxide | NaOH |
| Potassium hydroxide | KOH |
| Magnesium hydroxide | Mg(OH) 2 |
| Calcium hydroxide | Ca(OH) 2 |
All of the bases listed in the table are solids at room temperature., Po rozpuštění ve vodě se každý oddělí do kovového kationtu a hydroxidového iontu.
![]()
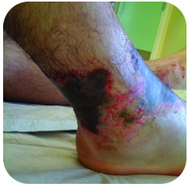
Obrázek 2. Tato noha má těžké popáleniny v důsledku dlouhodobého kontaktu s roztokem hydroxidu sodného, známého také jako louh.
hydroxid sodný je velmi žíravá látka známá také jako louh. Louh se používá jako přísný čistič a je složkou při výrobě mýdel. Je třeba dbát na silné báze, jako je hydroxid sodný, protože expozice může vést k těžkým popáleninám (viz Obrázek 2 ).,
sodík patří do skupiny prvků nazývaných alkalické kovy. Alkalický roztok je jiný název řešení, které je základní. Všechny alkalické kovy snadno reagují s vodou za vzniku hydroxidu kovu a vodíkového plynu. Výsledná řešení jsou základní.
Základny, které se skládají z alkalických kovů kation a hydroxidový anion jsou velmi dobře rozpustné ve vodě. Sloučeniny kovů skupiny 2 (kovy alkalických zemin) jsou také základní. Tyto sloučeniny však obecně nejsou tak rozpustné ve vodě., Proto jsou disociační reakce pro tyto sloučeniny zobrazeny jako rovnovážné reakce.
Tyto relativně nerozpustné hydroxidy byly některé ze sloučenin, které jsou diskutovány v souvislosti rozpustnost produkt je konstantní, ![]() . Rozpustnost hydroxidu hořečnatého je 0,0084 g na litr vody při 25°C.vzhledem k nízké rozpustnosti není hydroxid hořečnatý tak nebezpečný jako hydroxid sodný., Ve skutečnosti je hydroxid hořečnatý aktivní složkou produktu zvaného mléko magnézie, které se používá jako antacida nebo mírné projímadlo.
. Rozpustnost hydroxidu hořečnatého je 0,0084 g na litr vody při 25°C.vzhledem k nízké rozpustnosti není hydroxid hořečnatý tak nebezpečný jako hydroxid sodný., Ve skutečnosti je hydroxid hořečnatý aktivní složkou produktu zvaného mléko magnézie, které se používá jako antacida nebo mírné projímadlo.
souhrn
- kyselina Arrhenius je definována.
- jsou uvedeny příklady arrheniových kyselin.
- Arrheniova báze je definována.
- jsou uvedeny příklady arrheniových bází.
Cvičení
Přečtěte si materiál na níže uvedený odkaz a odpovězte na následující otázky:
http://dwb4.unl.edu/Chem/CHEM869R/CHEM869RLinks/www.nidlink.com/7Ejfromm/arrhenius.htm
- Co bylo Arrhenius první vědecké nápad?
- co si o tom myslel jeho Ph.D. výbor?,
- co pro tento nápad vyhrál?
- napište generickou rovnici pro disociaci kyseliny Arrhenius.
recenze
kyseliny Arrhenius
- co je kyselina Arrhenius?
- co je hydroniový iont?
- je H2SO4 monoprotická nebo polyprotická kyselina?
Arrhenius Bases
- co je Arrheniova základna?
- jaká je jedna reakce, která vytvoří arrheniovu základnu?
- jsou báze alkalických zemin velmi rozpustné ve vodě?
Leave a Reply