nucleul unui atom este înconjurat de electroni care ocupă cochilii sau orbite de diferite niveluri de energie.
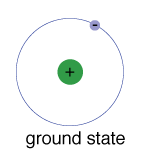
starea De bază a unui electron, nivelul de energie se normallyoccupies, este statul cel mai mic de energie pentru că electron.
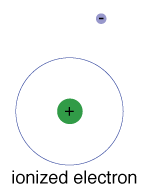
există, de asemenea, o energie maximă pe care fiecare electron o poateau și încă fac parte din atomul său., Dincolo de această energie, electronis nu mai este legat de nucleul atomului și este considerat tobe ionizat.când un electron ocupă temporar o stare de energie mai mare decâtstarea sa la sol, este într-o stare excitată. Un electron poatedeveniți excitat dacă i se dă energie suplimentară, cum ar fi dacă absoarbe un foton sau un pachet de lumină sau se ciocnește cu un atom sau particulă din apropiere.
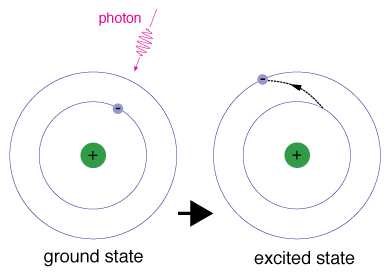
fiecare orbital are o energie specifică asociată cu acesta., Pentru anelectron să fie stimulat la un orbital cu energie mai mare, se mustovercome diferența de energie între orbital în care se găsește și theorbital la care se merge. Aceasta înseamnă că trebuie să absoarbă un fotoncare conține exact acea cantitate de energie sau să ia exact astacantitatea de energie dintr-o altă particulă într-o coliziune.electronii nu rămân în stări excitate de foarte mult timp-în curândreveniți la stările lor terestre, emițând un foton cu aceeași energie ca și cea absorbită.,

Tranziții între diferitele orbitali sunt unice pentru fiecare elementbecause nivelurile de energie sunt unic determinate de protoni andneutrons în nucleu. Când electronii de un anumit atom revenicu mai mici orbitali de stari excitate, fotonii se emit haveenergies, care sunt caracteristice de acest tip de atom. Acest lucru conferă fiecărui element o amprentă unică, făcând posibilă identificarea elementelor prezente într-un recipient de gaz sau chiar o stea.
Actualizat: noiembrie 2013
Leave a Reply