Oppimisen Tavoitteet
- Määritä Arrheniuksen happo.
- anna esimerkkejä Arrheniuksen hapoista.
- kuvaa hydroniumionia.
- Määrittele Arrheniuksen tukikohta.
- anna esimerkkejä Arrheniuksen tukikohdista.
Arrheniushapot
eivät hengitä liian syvään.
 Venus on planeetta jotka ovat meitä lähimpänä, mutta on hyvin erilainen ja vihamielinen ympäristö.
Venus on planeetta jotka ovat meitä lähimpänä, mutta on hyvin erilainen ja vihamielinen ympäristö.
sen pintalämpötila on noin 450°C., Ilmakehä koostuu hiilidioksidista, mutta rikkihappopilvet liikkuvat ylemmässä ilmakehässä auttaen luomaan äärimmäisen epäystävälliset olosuhteet. Näiden olosuhteiden vuoksi Venus ei ole paikka, jossa haluat vierailla lomalla.
Arrhenius Hapot
ruotsalainen kemisti Svante Arrhenius (1859-1927) oli ensimmäinen ehdottaa teoria selittää havaittu käyttäytyminen hapot ja emäkset. Koska ne pystyvät johtamaan virtaa, hän tiesi, että sekä hapot että emäkset sisälsivät ioneja liuoksessa., Arrheniushappo on yhdiste, joka ionisoituu tuottamaan vesiliuoksessa vetyioneja (H+).
hapot ovat molekyyliyhdisteitä, joissa on ionisoituvia vetyatomeja. Vain erittäin polaariseen kovalenttiseen sidokseen kuuluvat vetyatomit ovat ionisoituvia. Vetykloridi (HCl) on kaasu huoneenlämmössä ja normaalissa paineessa. Vetykloridin h-Cl-sidos on polaarisidos. Vetyatomi on elektronipuutos klooriatomin korkeamman elektronegatiivisuuden vuoksi., Näin vetyatomi vetää puoleensa vesimolekyylin yksinäistä elektroniparia, kun HCl liukenee veteen. Tuloksena on, että H-Cl-sidos hajoaa, jolloin molemmat sidoselektronit pysyvät Cl: n mukana muodostaen kloridi-ionin. H + – ioni kiinnittyy vesimolekyyliin muodostaen hydroniumioniksi kutsutun polyatomisen ionin. Se hydronium-ioni (H 3 O + ) voi olla ajatellut koska vesimolekyyli, jossa on kiinnitetty vety-ioni.

Kuva 1. Hydroniumionin muodostuminen.,
Yhtälöt osoittaa ionisaatio happo vesi on usein yksinkertaistettu jättämällä vesimolekyyli:
![]()
Tämä on pelkkä yksinkertaistaminen edellinen yhtälö, mutta se on yleisesti käytetty. Mahdolliset vety-ioneja vesiliuoksessa on kiinnitetty vesimolekyylien hydronium-ioneja.
 kaikki molekyyliyhdisteiden vetyatomit eivät ole ionisoituvia. Metaani (CH 4 ), vetyatomit ovat kovalenttisesti sitoutunut hiili sidoksia, jotka ovat vain hieman polar., Vetyatomit eivät kykene ionisoitumaan, eikä metaanilla ole happamia ominaisuuksia. Etikkahappo (CH 3 COOH) kuuluu happojen luokkaan, jota kutsutaan orgaanisiksi hapoiksi. Molekyylissä on neljä vetyatomia, mutta vain yksi happiatomiin sitoutunut vety on ionisoituva.
kaikki molekyyliyhdisteiden vetyatomit eivät ole ionisoituvia. Metaani (CH 4 ), vetyatomit ovat kovalenttisesti sitoutunut hiili sidoksia, jotka ovat vain hieman polar., Vetyatomit eivät kykene ionisoitumaan, eikä metaanilla ole happamia ominaisuuksia. Etikkahappo (CH 3 COOH) kuuluu happojen luokkaan, jota kutsutaan orgaanisiksi hapoiksi. Molekyylissä on neljä vetyatomia, mutta vain yksi happiatomiin sitoutunut vety on ionisoituva.
O-H-sidos voidaan ionisoida tuottamaan H + – ioni ja asetaatti-ioni. Tämän molekyylin muut vetyatomit eivät ole happamia.,e common acids:
| Acid Name | Formula |
| Hydrochloric acid | HCl |
| Nitric acid | HNO 3 |
| Sulfuric acid | H 2 SO 4 |
| Phosphoric acid | H 3 PO 4 |
| Acetic acid | CH 3 COOH |
| Hypochlorous acid | HClO |
A monoprotic acid is an acid that contains only one ionizable hydrogen., Suolahappo ja etikkahappo ovat monoproottisia happoja. Polyproottinen happo on happo, joka sisältää useita ionisoituvia vetyjä. Yleisin polyprotic hapot ovat joko diprotic (kuten H 2 SO 4 ) tai triprotic (kuten H 3 PO 4 ).
Arrheniuksen tukikohdat
mihin tätä voidaan käyttää?

natriumhydroksidi on monipuolinen kemian. Sitä voidaan käyttää niin arkisiin tarkoituksiin kuin tukkeutuneiden viemärien puhdistamiseen. Useat kaupalliset valmisteet sisältävät tähän tarkoitukseen natriumhydroksidia. Sillä on myös useita sovelluksia elintarviketeollisuuden alalla., Jäätelö paksuuntuu NaOH: lla. Jos oliiveja liotetaan natriumhydroksidia ja muita kemikaaleja sisältävässä liuoksessa, oliivit muuttuvat mustiksi. Pehmeät suolarinkelit tehdään pureskeltaviksi lisäämällä ruokaan natriumhydroksidia. Tämä yhdiste on laajalti käytetty synteesissä muovit, etsaus alumiini, maalin poisto, ja työskentelee sarvien poistamista karjaa (siinä tapauksessa, että on tarvetta sinulla on).
Arrhenius Emäkset
On Arrheniuksen emäs on yhdiste, joka ionizes tuottaa hydroksidi-ioneja (OH− ) vesiliuoksessa., The Table below lists several of the more common bases:
| Base Name | Formula |
| Sodium hydroxide | NaOH |
| Potassium hydroxide | KOH |
| Magnesium hydroxide | Mg(OH) 2 |
| Calcium hydroxide | Ca(OH) 2 |
All of the bases listed in the table are solids at room temperature., Veteen liuetessaan kukin hajoaa metallikationiksi ja hydroksidi-ioniksi.
![]()
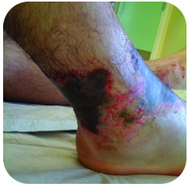
Kuva 2. Tällä jalalla on vakavia palovammoja, jotka johtuvat pitkäaikaisesta kosketuksesta natriumhydroksidiliuokseen, joka tunnetaan myös lipeänä.
natriumhydroksidi on hyvin Kaustinen aine, jota kutsutaan myös lipeäksi. Lipeää käytetään tiukkana puhdistusaineena ja se on ainesosa saippuoiden valmistuksessa. On noudatettava varovaisuutta vahvojen emästen, kuten natriumhydroksidin, kanssa, sillä altistuminen voi johtaa vakaviin palovammoihin (KS.kuva 2).,
natrium kuuluu alkalimetalleiksi kutsuttujen alkuaineiden ryhmään. Emäksinen liuos on perusratkaisulle toinen nimi. Kaikki alkalimetallit reagoivat helposti veden kanssa tuottaakseen metallihydroksidia ja vetykaasua. Tuloksena olevat ratkaisut ovat perusratkaisuja.
Emäkset, jotka koostuvat alkali-metalli-kationien ja hydroksidi-anioni ovat kaikki liukenee erittäin hyvin veteen. Myös ryhmän 2 metallien yhdisteet (emäksiset maametallit) ovat emäksisiä. Nämä yhdisteet eivät kuitenkaan yleensä ole yhtä liukoisia veteen., Siksi näiden yhdisteiden dissosiaatioreaktiot esitetään tasapainoreaktioina.
Nämä suhteellisen liukenemattomia hydroksideja olivat joitakin yhdisteitä keskusteltu yhteydessä liukoisuus tuotteen jatkuva ![]() . Liukoisuus magnesiumhydroksidi on 0.0084 g / l vesi at 25°C. Koska sen alhainen liukoisuus, magnesiumhydroksidi ei ole yhtä vaarallinen kuin natriumhydroksidi., Itse asiassa, magnesiumhydroksidi on aktiivinen ainesosa tuotteen nimeltä maitoa magnesia, jota käytetään antasidi tai lievä laksatiivinen.
. Liukoisuus magnesiumhydroksidi on 0.0084 g / l vesi at 25°C. Koska sen alhainen liukoisuus, magnesiumhydroksidi ei ole yhtä vaarallinen kuin natriumhydroksidi., Itse asiassa, magnesiumhydroksidi on aktiivinen ainesosa tuotteen nimeltä maitoa magnesia, jota käytetään antasidi tai lievä laksatiivinen.
Yhteenveto
- Arrheniuksen happo on määritelty.
- esimerkkejä Arrhenius-hapoista annetaan.
- Arrheniuksen tukikohta on määritelty.
- esimerkkejä Arrheniuksen tukikohdista on annettu.
Käytäntö
Lue materiaali alla olevasta linkistä ja vastaa seuraaviin kysymyksiin:
http://dwb4.unl.edu/Chem/CHEM869R/CHEM869RLinks/www.nidlink.com/7Ejfromm/arrhenius.htm
- Mikä oli Arrhenius’ ensimmäinen tieteellinen idea?
- mitä mieltä hänen tohtorin komiteansa oli siitä?,
- mitä hän voitti tästä ideasta?
- Kirjoita yleinen yhtälö dissosiaatio on Arrheniuksen happo.
Arvostelu
Arrhenius Hapot
- Mitä on Arrheniuksen happo?
- mikä on hydroniumioni?
- onko H2SO4 monoproottinen vai polyproottinen happo?
Arrheniuksen tukikohdat
- mikä on Arrheniuksen tukikohta?
- mikä on yksi reaktio, joka muodostaa Arrheniuksen tukikohdan?
- ovatko emäksiset maaemäkset hyvin vesiliukoisia?
Leave a Reply